Надоело покупать пакетики к фотометру Hanna... не то чтобы шибко дорого, порядка 50 рублей за тест на текущий момент, но лишний раз не перепроверишь, пакетик жалко, и вечно когда надо кончаются. Короче, без долгого вступления, давно я собирался окончательно решить вопрос с тестом на фосфат, так чтобы один раз купить реактивы и на всю жизнь. Hanna использует стандартный метод определения фосфатов с образованием молибденовой сини - в состав ее пакетиков входит молибденовокислый аммоний, соль сурьмы, аскорбиновая кислота и что-то подкисляющее все это дело. Методика подробно описана в официальных руководствах по анализу, например вот http://docs.cntd.ru/...ment/1200056718, а также, с небольшими изменениями видел ее же в книгах по химанализу морской воды, например в этой: "A practical handbook of seawater analysis" http://www.dfo-mpo.g...ibrary/1507.pdf
Итак, необходимые реактивы:
1) Молибдат аммония - у меня откуда-то была банка, купить не проблема, у многих, кто удобрения делал, он есть.
2) Аскорбиновая кислота, она же витамин С, порошок - можно в аптеке, но я купил на ebay - в строку поиска вбить " Ascorbic Acid", куча предложений.
3) Антимонилтартрат калия. - Купил на ebay (английское название Potassium antimony(III) tartrate hydrate).
4) Серная кислота. У меня была бутылка. Не знаю можно ли сейчас где ее купить (концентрированную), не уверен пойдет ли аккумуляторная (не знаю насколько она чистая, вдруг в ней фосфаты есть, надо пробовать). По информации с интернета ее можно с успехом заменить на, например, гидросульфат калия KHSO4. В принципе она нужна только для создания кислой среды, в пакетиках Ханны для этого используется какая-то кислая соль (может тот же гидросульфат калия, может что-то другое, кислое).

В пакетиках от Ханны все эти реактивы отвешены в нужном количестве. Нам бы тоже, для простоты, смешать сухие порошки... но боюсь смесь расслаиваться будет - короче, кому интересно, пробуйте сами, а я делал по официально утвержденной методике, в которой сказано, что следует делать растворы:
Из реактивов делаем растворы:
1). Серная кислота - 140мл концентрированной кислоты на 900мл воды (кислоту льем в воду, а не наоборот, иначе вскипит!). Видимо, можно изначально взять разбавленную кислоту. Или использовать кислые соли, как я написал выше.
2). Mолибдат аммония - 15гр в 500мл осмоса. (Хранится неопределенно долго.)
3) Антимонилтартат - 0.34гр в 250мл осмоса. Раствор не портится.
4). Аскорбиновая кислота - 2.7гр в 50 мл осмоса. Нет смысла делать много этого раствора, он портится, а чтоб дольше не портился можно хранить в холодильнике. Можно даже заморозить.
Повторюсь - в пакетиках Ханны почти то же самое, но в сухом виде, поэтому хорошо хранится. А нам придется смешивать растворы перед употреблением ![]() , смешанный реактив на фосфат портится в течение примерно 6 часов.
, смешанный реактив на фосфат портится в течение примерно 6 часов.
Смешанный реактив на фосфат:
в маленький стаканчик отмеряем шприцем:
Раствор 1 (кислота) - 5мл
Раствор 2 (молибдат) - 2мл
Раствор 3 (антимонил) - 1мл
Раствор 4 (аскорбинка) - 2мл
Получается желтоватый раствор, на фото ниже в стаканчике слева. Использовать в течение 6 часов, потом можно вылить.
Измерение фосфата:
В Ханновкую пробирку воду из аквариума до риски (10мл),
влить Смешанный реактив на фосфат - 1мл
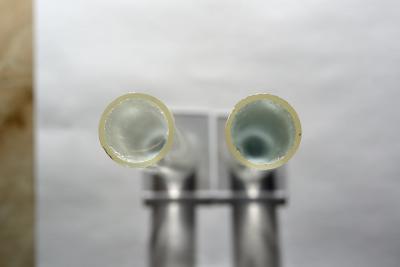
При наличии фосфатов окрашивается в синий цвет в течение 5 минут. Окраска стабильна как минимум пару часов. Так что 5 минут подождали и можно измерять - включаем Ханну, вставляем пробирку с чистой водой, она устанавливается на ноль, затем пробирку с тестируемой водой, сразу измеряем (таймер не нужен).

Удивительно, но несмотря на не родные реактивы, ханна показывает циферки очень близкие к делу. В любом случае всегда можно сделать калибровочный раствор (из гидрофосфата калия например, K2HPO4) и откалиброваться по нему.
Кроме того, так как теперь мы не ограничены в реактивах и не платим по 50 рублей за каждый тест, то возможны различные варианты для тех, у кого нет Ханны. Например проводить тест с бОльшим количеством воды в высоких пробирках и смотреть на окраску сверху - в толстом слое воды синяя окраска от фосфатов будет гораздо лучше видна, чем в ханновских пробирках.
Отредактировано 22.05.2016:
Изменена последовательность смешивания реактивов, оказалось это важно. Смешивают в такой последовательности: кислота, молибдат, антимонил, аскорбинка.
Капать растворы в пробу воды по отдельности нельзя, сначала готовят смешанный реактив, затем только добавляют его в пробу воды.
Еще важный момент - хранить раствор молибдата надо в пластиковой бутылке (не в стекле), иначе он тянет со стекла силикат и показывает завышенные значения.
Тест на силикат в сообщении #46